年内股價翻倍!雲頂新耀基本面驅動價值回歸?
12月3日,雲頂新耀-B(01952.HK)延續近期上漲勢頭,盤中最高飙漲15.27%。截至收盤,其股價漲幅為10.96%,報45.05港元。
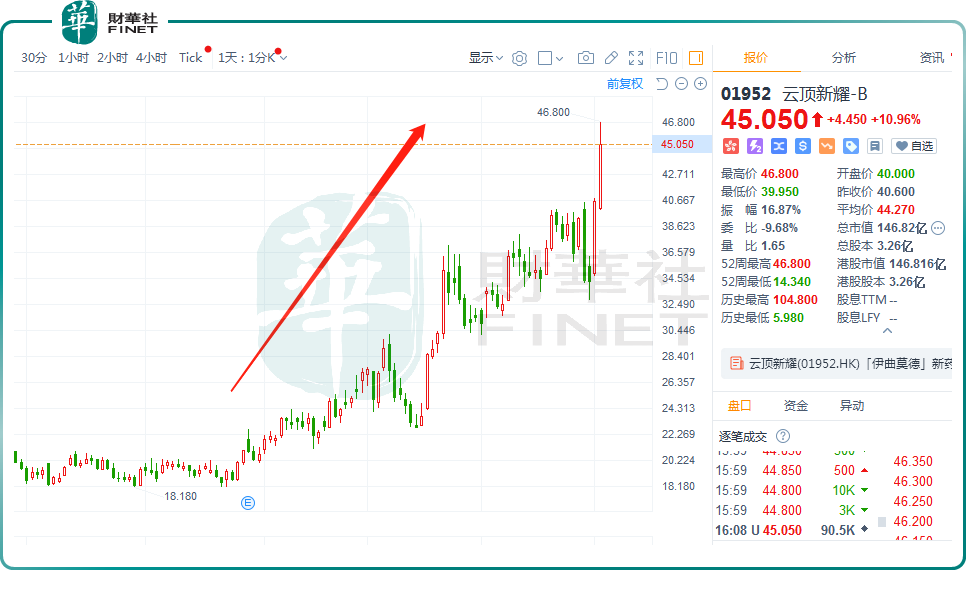
拉長周期看,自8月下旬至今,該股走勢頗為陡峭,區間累計漲幅達1.4倍;年内累漲115.55%,表現優於同行,引發市場廣泛關注。
資料顯示,雲頂新耀已發展成為一家從早期研發、臨床開發、注冊、生產到商業化的全產業鏈綜合性生物制藥公司,其研發領域包括腎科疾病、mRNA技術、感染性及傳染性疾病、自身免疫性疾病等。
深入分析,雲頂新耀股價所呈現出的高漲態勢,這背後固然有整體行情的因素,但更重要的是公司新產品商業化提速,進一步增強了市場對雲頂新耀未來業績的樂觀預期。
消息面上,近期,雲頂新耀公司旗下兩款重磅產品,耐賦康®和伊曲莫德,均取得了重要進展。
11月28日,雲頂新耀宣佈耐賦康(佈地奈德腸溶膠囊,NEFECON)成功納入國家醫保藥品目錄。新版國家醫保藥品目錄將於2025年1月1日起正式生效。
耐賦康為全球首個獲得美國食品藥品監督管理局和歐洲藥品管理局完全批準的IgA腎病治療藥物,於2023年11月通過優先審評程序正式獲得中國國家藥品監督管理局批準,用於治療原發性IgA腎病的成年患者,是中國唯一獲得IgA腎病適應症的治療藥物。
資料顯示,IgA腎病是我國最常見的原發性腎小球疾病,以18-45歲的青壯年為主要發病人群。目前我國約有500萬IgA腎病患者,且每年新增確診患者超過10萬人。這是一個極其龐大的治療市場基礎。
納入醫保目錄後,耐賦康的放量邏輯將愈發清晰,即以更高的可負擔性,惠及更多患者。可以預見,明後年銷售將會加速放量,有望助力公司業績提升。
此外,雲頂新耀在自免疫領域的重磅藥品——伊曲莫德(VELSIPITY)也即將迎來收獲期。
近日,雲頂新耀宣佈伊曲莫德(VELSIPITY)用於治療中重度活動性潰瘍性結腸炎成人患者的新藥上市許可申請,已獲得香港衛生署正式受理。該產品已於今年4月獲得澳門藥物監督管理局批準上市,並於10月份通過「港澳藥械通」政策在大灣區落地。
伊曲莫德,是歐盟首個且唯一獲批用於16歲及以上患者的新一代口服治療中重度活動性潰瘍性結腸炎藥物,也是目前唯一在全球Ⅲ期臨床試驗中證實對孤立性直腸炎有療效的藥物。
近年來,潰瘍性結腸炎在我國發病率明顯增加,預計到2030年,中國的潰瘍性結腸炎患者人數預計將達到約100萬人,存在迫切且巨大的未被滿足的臨床需求。
華福證券表示,伊曲莫德很大潛力成為中國中度至重度潰瘍性結腸炎的一線治療藥物,可口服給藥,無安全性黑框標簽,展現出與生物制劑相當的臨床療效,預計24 年内在中國内地遞交NDA 申請。
需要指出的是,雖然雲頂新耀在產品線方面頻頻迎來好消息,但其依舊未擺脫虧損,且上半年虧損進一步擴大。
根據財務數據顯示,2024年上半年,雲頂新耀收入3.02億元,同比增長高達32.9倍。儘管公司收入大幅增長,但其仍深陷虧損泥淖。期内,其錄得歸母淨虧損約6.32億元,而上年同期則虧損4.24億元,虧損進一步擴大。
不過,對於生物醫藥企業而言,早期往往依賴於大量的研發投入,初期虧損並不代表未來業績不會改善。
展望後市,伴隨著多款重磅產品商業化持續提速,市場普遍認為,雲頂新耀的業績有望迎來持續增長,逐漸實現扭虧為盈。



